Τι είναι η μεσογειακή αναιμία;
Τι είναι η μεσογειακή αναιμία;
Ο όρος μεσογειακή αναιμία χρησιμοποιείται συχνά ως συνώνυμος του όρου θαλασσαιμία και με αυτόν περιγράφουμε μία ομάδα κληρονομικών νόσων, που χαρακτηρίζονται από ελαττωματική παραγωγή αιμοσφαιρίνης. Ο όρος «θαλασσαιμία» προέρχεται – προφανώς – από τη λέξη «θάλασσα», διότι η κλινική αυτή οντότητα για πρώτη φορά περιγράφηκε μεταξύ πληθυσμών, που ζουν πέριξ της Μεσογείου Θάλασσας. Εντούτοις, η συχνότητα της θαλασσαιμίας είναι υψηλή και σε περιοχές της Μέσης Ανατολής, της Αφρικής και της Ασίας (National Center for Biotechnology Information, 1998).
Γιατί παρουσιάζεται η θαλασσαιμία;
Η αιμοσφαιρίνη είναι η πρωτεΐνη του αίματος, που είναι «επιφορτισμένη» με τη μεταφορά του οξυγόνου από τους πνεύμονες στους ιστούς και εντοπίζεται εντός των κυττάρων του αίματος, που ονομάζονται ερυθρά αιμοσφαίρια. Η αιμοσφαιρίνη με τη σειρά της αποτελείται από δύο ζεύγη πρωτεϊνικών αλυσίδων (πιο «σωστός» είναι ο όρος «πολυπεπτιδικών αλυσίδων»): ένα ζεύγος αλυσίδων α και ένα ζεύγος αλυσίδων β. Κάθε αλυσίδα είναι συνδεδεμένη με ένα μόριο Αίμης καθώς και ένα άτομο Σιδήρου (βλ. εικόνα).
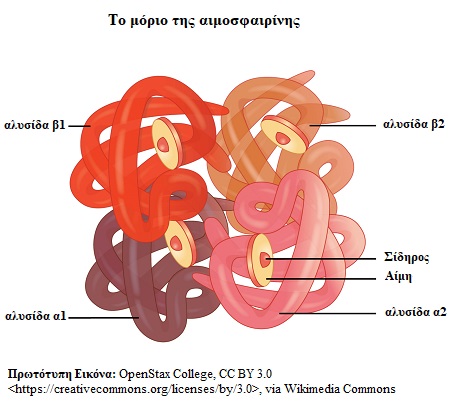
Ανάλογα με το αν το γονίδιο, που φέρει την παθολογική μετάλλαξη και κωδικοποιεί για την α ή τη β αλυσίδα της αιμοσφαιρίνης, οι θαλασσαιμίες διακρίνονται σε α και β θαλασσαιμίες. Στην Ελλάδα η συντριπτικά συνηθέστερη θαλασσαιμία, που απαντάται είναι η β θαλασσαιμία. Έχει υπολογιστεί, πως στην περιοχή της Ελλάδος, της Κύπρου και της Τουρκίας μάλιστα το ποσοστό των «φορέων» φθάνει κατά περιοχή και το 15% (Needs και συνεργάτες, 2023). Με αυτή τη μορφή θαλασσαιμίας θα ασχοληθούμε στο πόνημα αυτό.
Πώς επηρεάζεται η υγεία της εγκύου από τη Μεσογειακή αναιμία;
Στο σημείο αυτό θα πρέπει να γίνει διαχωρισμός μεταξύ:
• των γυναικών, που νοσούν από κάποια μορφή β θαλασσαιμίας
• των γυναικών, που είναι φορείς της β θαλασσαιμίας, έχουν δηλαδή το «στίγμα»
Πώς εξελίσσεται η εγκυμοσύνη μίας γυναίκας, που πάσχει από β θαλασσαιμία;
Οι ασθενείς με την ενδιάμεση μορφή β θαλασσαιμίας, παρουσιάζουν τα πρώτα σημεία αναιμίας μετά τη συμπλήρωση 2 ετών και κατά κανόνα δεν χρειάζεται να υποβάλλονται σε τακτικές μεταγγίσεις αίματος. Εντούτοις, παρουσιάζουν δομικές διαταραχές σε διάφορα όργανα του σώματός τους (σπλήνας, ήπαρ, λεμφαδένες), αλλά και στα οστά (θώρακας και σπονδυλική στήλη), τα οποία συχνά προσβάλλονται από οστεοπόρωση. Επίσης τα άτομα αυτά συχνά εμφανίζουν χολολιθίαση (δημιουργία λίθων στη χοληδόχο κύστη) και έντονη προδιάθεση για την εκδήλωση θρομβώσεων (Origa & Comitini, 2019). Η πιθανότητα θρομβώσεων κατά τη διάρκεια της κύησης είναι και από τις βασικότερες επιπλοκές, που συνδέονται με την παθολογία αυτή (Petrakos και συνεργάτες, 2016).
Τα άτομα με μείζονα Μεσογειακή Αναιμία χρειάζονται μεταγγίσεις σε τακτικά χρονικά διαστήματα. Η διαδικασία της μετάγγισης όμως συνδέεται με υπερβολική αύξηση της ποσότητας σιδήρου, που εντοπίζεται στο σώμα. Ο σίδηρος επικάθεται σε διάφορα όργανα του σώματος, στα οποία και προκαλεί ιστική βλάβη. Το βασικότερο εκ των οργάνων, που βλάπτονται από το σίδηρο σε τέτοιες περιπτώσεις είναι η καρδιά. Για το λόγο αυτό χορηγούνται στα άτομα αυτά φαρμακευτικές ουσίες, που προκαλούν την απομάκρυνση του υπερβάλλοντος σιδήρου από το αίμα μέσω της ούρησης. Τέτοιου είδους ουσίες ονομάζονται χηλικοί παράγοντες (Origa & Comitini, 2019).
Οι χηλικοί παράγοντες κατά κανόνα δεν συστήνεται να χορηγούνται διαρκούσης της κύησης, αφού μελέτες σε αρουραίους κατέδειξαν ενδεχόμενη τερατογόνο δράση τους, αν και μελέτες σε άλλα ζώα δεν επιβεβαίωσαν τη δράση αυτή. Δεν υπάρχουν πάντως στοιχεία για ενδεχόμενη δυσμενή επίδραση των ουσιών αυτών στο έμβρυο του ανθρώπου. Εντούτοις, φαίνεται, πως τα πλεονεκτήματα της επανέναρξης της χορήγησης χηλικών παραγόντων προς το τέλος του δευτέρου τριμήνου είναι μία πρακτική, της οποίας τα πλεονεκτήματα υπερτερούν των όποιων κινδύνων (Origa & Comitini, 2019).
Συχνά, σε ό,τι αφορά γυναίκες με β θαλασσαιμία, που χρήζουν τακτικών μεταγγίσεων, των οποίων η καρδιακή λειτουργία είναι ικανοποιητική, ακολουθείται η μέθοδος της έντονης χηλικοποίησης (= χορήγηση χηλικών παραγόντων) πριν την εγκυμοσύνη με τακτική παρακολούθηση της καρδιακής λειτουργίας κατά τη διάρκεια της κύησης (Petrakos και συνεργάτες, 2016). Εν πάσει περιπτώσει ο κίνδυνος καρδιακής βλάβης εξαιτίας της υπερβολικής συγκέντρωσης σιδήρου κατά τη διάρκεια της κύησης είναι ιδιαίτερα υψηλός και για το λόγο αυτό είναι απαραίτητη η στενή παρακολούθηση της καρδιακής λειτουργίας και η άμεση επανέναρξη της αγωγής με χηλικούς παράγοντες μετά τον τοκετό (Vlachodimitropoulou και συνεργάτες, 2024).
Μία ακόμα παράμετρος, που κατά κανόνα παρακολουθείται στενά κατά τη διάρκεια της κύησης, όταν η γυναίκα πάσχει από β θαλασσαιμία, που χρήζει μεταγγίσεων, είναι ο δείκτης της συγκέντρωσης της αιμοσφαιρίνης στο αίμα. Η υπερβολικά χαμηλή συγκέντρωση αιμοσφαιρίνης έχει συνδεθεί με αυξημένες πιθανότητες για πρόωρο τοκετό, αλλά και για τη γέννηση λιποβαρούς νεογνού. Γενικά, προβαίνουμε σε μετάγγιση της γυναίκας, όταν η συγκέντρωση αιμοσφαιρίνης πέφτει κάτω από τα 10g/dL (Origa & Comitini, 2019).
Σε κάθε περίπτωση η κύηση μίας γυναίκας, που πάσχει από Μείζονα ή Ενδιάμεση Μεσογειακή Αναιμία θεωρείται υψηλού κινδύνου και απαιτείται η παρακολούθησή της από ομάδα ιατρών διαφόρων ειδικοτήτων.
Πώς εξελίσσεται η εγκυμοσύνη γυναικών, που έχουν το στίγμα Μεσογειακής Αναιμίας;
Κατά κανόνα, οι γυναίκες, που έχουν το στίγμα Μεσογειακής Αναιμίας φέρουν σε πέρας την εγκυμοσύνη τους χωρίς ιδιαίτερα προβλήματα (Tsatalas και συνεργάτες, 2009; Amooee και συνεργάτες, 2011). Όμως έχει καταγραφεί, πως ενδεχομένως να διατρέχουν σχετικά υψηλότερο κίνδυνο για εκδήλωση αναιμίας και υπερτασικών διαταραχών κατά την κύηση (Ruangvutilert και συνεργάτες, 2022).
Δείτε ΕΔΩ σε ποιο στάδιο της κύησης βρίσκεστε!
Δρ ΜΕΝΕΛΑΟΣ ΚΩΝ. ΛΥΓΝΟΣ, MSc, PhD
ΜΑΙΕΥΤΗΡ ΧΕΙΡΟΥΡΓΟΣ ΓΥΝΑΙΚΟΛΟΓΟΣ
Master of Science University College London
Διδάκτωρ Μαιευτικής Γυναικολογίας
Ενδεικτική βιβλιογραφία
National Center for Biotechnology Information (US). Genes and Disease [Internet]. Bethesda (MD): National Center for Biotechnology Information (US); 1998-. Thalassemia. Available from: https://www.ncbi.nlm.nih.gov/books/NBK22200/
Needs T, Gonzalez-Mosquera LF, Lynch DT. Beta Thalassemia. [Updated 2023 May 1]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2024 Jan-. Available from: https://www.ncbi.nlm.nih.gov/books/NBK531481/
Origa R, Comitini F. Pregnancy in Thalassemia. Mediterr J Hematol Infect Dis. 2019 Mar 1;11(1):e2019019. doi: 10.4084/MJHID.2019.019. PMID: 30858957; PMCID: PMC6402552.
Petrakos G, Andriopoulos P, Tsironi M. Pregnancy in women with thalassemia: challenges and solutions. Int J Womens Health. 2016 Sep 8;8:441-51. doi: 10.2147/IJWH.S89308. PMID: 27660493; PMCID: PMC5019437.
Vlachodimitropoulou E, Mogharbel H, Kuo KHM, Hwang M, Ward R, Shehata N, Malinowski AK. Pregnancy outcomes and iron status in β-thalassemia major and intermedia: a systematic review and meta-analysis. Blood Adv. 2024 Feb 13;8(3):746-757. doi: 10.1182/bloodadvances.2023011636. PMID: 38181780; PMCID: PMC10847873.
Tsatalas C, Chalkia P, Pantelidou D, Margaritis D, Bourikas G, Spanoudakis E. Pregnancy in beta-thalassemia trait carriers: an uneventful journey. Hematology. 2009 Oct;14(5):301-3. doi: 10.1179/102453309X439791. PMID: 19843388.
Amooee S, Samsami A, Jahanbakhsh J, Karimi M. The pregnancy outcome in patients with minor β-thalassemia. Iran J Reprod Med. 2011 Winter;9(1):9-14. PMID: 25356075; PMCID: PMC4212139.
Ruangvutilert P, Phatihattakorn C, Yaiyiam C, Panchalee T. Pregnancy outcomes among women affected with thalassemia traits. Arch Gynecol Obstet. 2023 Feb;307(2):431-438. doi: 10.1007/s00404-022-06519-y. Epub 2022 Mar 26. PMID: 35347380; PMCID: PMC9918558.